Mẫu dò là một phân tử acid nucleic (ADN sợi đơn hoặc ARN sợi đơn) có ái lực mạnh với đích đặc hiệu (trình tự ADN hoặc ARN). Mẫu dò và trình tự base đích bổ sung cho nhau, nhưng tùy thuộc điều kiện, chúng không nhất thiết phải bổ sung hoàn toàn. Phân tử lai (kết hợp mẫu dò – đích) có thể được phát hiện khi một hệ thống xác định và đánh dấu thích hợp được sử dụng. Các mẫu dò gen thường được áp dụng trong nhiều kỹ thuật blotting và các kỹ thuật lai tại chỗ (in situ techniques) nhằm mục đích xác định các trình tự acid nucleic. Trong y học, chúng có thể giúp định danh vi sinh vật và chẩn đoán các bệnh di truyền, bệnh truyền nhiễm và nhiều dạng bệnh khác.
2. Thiết kế mẫu dò
Thiết kế mẫu dò phụ thuộc vào yêu cầu sử dụng mẫu dò gen hay mẫu dò oligonucleotide.
2.1. Mẫu dò gen (Gene Probes)
Mẫu dò gen thường dài hơn 500 base và chứa toàn bộ (hay phần lớn) trình tự gen đích.
Chúng có thể được tạo ra bằng hai cách:
2.2. Mẫu dò oligonucleotide (Oligonucleotide Probes)
Mẫu dò oligonucleotide có đích là các trình tự đặc hiệu bên trong gen. Kích thước phổ biến của loại mẫu dò này là 18 – 30 base. Tuy vậy, các thiết bị tổng hợp hiện nay cho phép thiết kế hiệu quả các mẫu dò chứa ít nhất 100 base. Mẫu dò oligonucleotide gắn chính xác với trình tự đích. Chiều dài của chúng phù hợp cho phản ứng lai trong các điều kiện ngặt nghèo, giúp xác định ADN với những khác biệt rất nhỏ trong trình tự. Quá trình lựa chọn mẫu dò oligonucleotide có thể thực hiện sử dụng từ những trình tự gen đã biết, theo những bước sau:
Tuy nhiên, để xác định điều kiện lai tối ưu, nên tiến hành lai mẫu dò với các acid nucleic đích đặc hiệu và không đặc hiệu trong phạm vi biến đổi lớn về điều kiện lai.
Quy trình tương tự được áp dụng thiết kế mồi xuôi và mồi ngược dùng trong phản ứng PCR. Chú ý rằng, trừ vùng cần khuếch đại, đầu 3’ của mồi xuôi và mồi ngược không tương đồng với các đoạn ADN khuôn khác.
3. Đánh dấu mẫu dò
3.1 Các kiểu đánh dấu
3.1.1. Đánh dấu phóng xạ (Radioactive Labels)
Mẫu dò acid nucleic có thể được đánh dấu bằng các đồng phân phóng xạ (32P, 35S, 125I, 3H) và xác định bằng ảnh X– ray hay hệ thống Geiger– Muller. Trước đây, mẫu dò đánh dấu phóng xạ được sử dụng rất phổ biến, nhưng với những lo ngại về tính an toàn cũng như giá cả và vấn đề chất thải phóng xạ, ngày nay, người ta ít sử dụng chúng. Đây là loại mẫu dò có độ nhạy và độ phân giải cao nhất. Chỉ một lượng nhỏ sản phẩm lai mẫu dò– đích cũng có thể được phát hiện, ví dụ: mẫu dò đánh dấu 32P có khả năng xác định các bản sao của gen trong 0.5 µg ADN. Keller and Manak đã giải thích như sau:
Mặc dù mẫu dò loại này giúp phát hiện lượng nhỏ ADN đích (< 1pg), nhược điểm của chúng là thời gian bán hủy ngắn (chỉ sử dụng trong vòng 1 tuần sau khi chuẩn bị) và không thể sử dụng cho kỹ thuật hình ảnh độ phân giải cao. So với 32P, năng lượng thấp và thời gian bán hủy dài khiến đồng phân 35S ổn định và ít đặc hiệu hơn. Mẫu dò đánh dấu 35S dù có độ nhạy thấp hơn nhưng cho hình ảnh X – ray với độ phân giải cao hơn và đặc biệt thích hợp sử dụng trong kỹ thuật lai tại chỗ. Một ưu điểm khác của nucleotide đánh dấu 35S là ít độc hơn so với 32P. Các hạt b năng lượng thấp gần như không thâm nhập vào lớp da chết phía trên và dễ dàng được thu lại bằng các ống, lọ thí nghiệm. Tương tự, mẫu dò đánh dấu 3H đã và đang được sử dụng trong lai tại chỗ vì chúng phát ra các hạt β năng lượng thấp, kết quả là độ tương phản đạt cực đại và tín hiệu nhiễu thấp, chúng cũng có thời gian bán hủy dài nhất (12.3 năm). Việc sử dụng125I và 131I giảm kể từ những năm 1970 do sự sẵn có của mẫu dò triphosphate nucleoside đánh dấu 125I với tính đặc hiệu cao. 125I có năng lượng thấp hơn và thời gian bán hủy dài hơn (60 ngày) so với 131I, thường được sử dụng trong lai tại chỗ.
3.1.2. Đánh dấu không phóng xạ
So với đánh dấu phóng xạ, sử dụng các dấu chuẩn không phóng xạ có một vài ưu điểm:
Một số dấu chuẩn trong đánh dấu không phóng xạ:

Hệ thống FISH
Một số vấn đề trong thiết kế mẫu dò cho FISH:
Tín hiệu được xác định với cơ chất tạo màu hay phát quang của alkaline phosphatase. Nếu sử dụng cơ chất tạo màu, tín hiệu hình thành trực tiếp trên màng. Trường hợp cơ chất phát quang, dùng phim X – ray để hiện tín hiệu.
Bảng 1. Các kiểu đánh dấu

3.2. Phương pháp đánh dấu
3.2.1. Phản ứng dịch chuyển điểm cắt (Nick Translation)
Phản ứng dịch chuyển điểm cắt là một phương pháp đánh dấu ADN, trong đó sử dụng các enzym DNase I tuyến tụy và Escherichia coli DNA polymerase I. Trong phản ứng, DNase I cắt mạch ADN ở một vài điểm (nick) và E. coli DNA polymerase I sẽ thêm nucleotide vào vị trí 3'-OH lộ ra ở các điểm cắt đó, đồng thời hoạt động 5’ - 3' exonuclease sẽ loại bỏ nucleotide ở đầu 5’. Nếu nucleotide đánh dấu đã có trong phản ứng, các nucleotide này sẽ tham gia vào mạch ADN. Đối với các ADN đánh dấu phóng xạ, [α-32P] dNTP sẽ được bổ sung. Đối với mẫu dò không phóng xạ, digoxigenin hoặc một đầu biotin gắn với một phân tử tương tự dNTP sẽ được sử dụng.
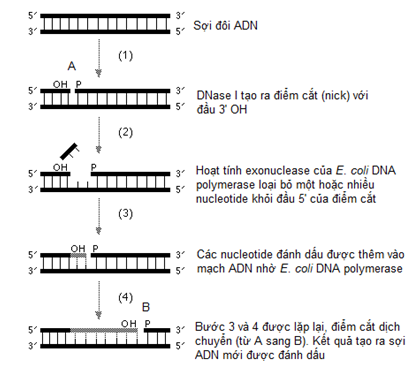
Phản ứng dịch chuyển điểm cắt (Nick Translation)
3.2.2. Đánh dấu bằng mồi ngẫu nhiên/ Kéo dài mồi (Random-Primed Labeling/ Primer Extension)
Mẫu dò gen (nhân dòng hay khuếch đại PCR), mẫu dò oligonucleotide có thể được đánh dấu bằng mồi ngẫu nhiên với các đồng phân phóng xạ và không phóng xạ (ví dụ DIG). Phân tử ADN sợi đôi trải qua quá trình biến tính và kết hợp với các đoạn mồi oligonucleotide ngẫu nhiên (6-mers). Các oligonucleotide này đóng vai trò như mồi cho 5' - 3' polymerase (đoạn Klenow). Mẫu dò đánh dấu được tổng hợp nhờ enzyme này khi trong môi trường có các nucleotide đánh dấu. Hình A thể hiện các bước trong đánh dấu DIG bằng mồi ngẫu nhiên.

Hình. (A). Đánh dấu DIG bằng mồi ngẫu nhiên. ADN sợi đôi bị biến tính và gắn mồi oligonucleotide ngẫu nhiên (6-mers); oligonucleotide này đóng vai trò như mồi cho đoạn Klenow của E. coli DNA polymerase I, enzyme sẽ tổng hợp mẫu dò đánh dấu DIG–dUTP. (B). Đánh dấu DIG bằng phản ứng PCR: DIG–dUTP tham gia mạch ADN trong quá trình khuếch đại khuôn ADN đích. Dấu hoa thị biểu hiện phân tử digoxigenin.
3.2.3. Đánh dấu DIG bằng phản ứng PCR (DIG–PCR Labeling)
Đây là một phương pháp tiên tiến đánh dấu mẫu dò gen với DIG sử dụng phản ứng PCR. Mẫu dò được khuếch đại sử dụng mồi phù hợp, tuy nhiên, hỗn hợp dNTP chứa ít dTTP vì DIG–dUTP cũng được thêm vào phản ứng này. Ưu điểm phương pháp này là gắn nhiều đuôi DIG dọc mạch ADN trong suốt quá trình khuếch đại. Hình B thể hiện các bước trong quá trình đánh dấu DIG bằng phản ứng PCR.
3.2.4. Đánh dấu photobiotin (Photobiotin Labeling)
Đánh dấu photobiotin là một phản ứng hóa học, không chỉ đơn giản là phản ứng enzyme. Biotin và DIG nối với một nhóm nitrophenyl azide. Nhóm này sẽ biến đổi bởi sự phát xạ với tia UV hoặc ánh sáng nhìn thấy, tạo phân tử nitrene hoạt động mạnh. Nhóm này có thể tạo liên kết cộng hóa trị vững chắc với ADN và ARN. Các vật liệu để đánh dấu photobiotin bền hơn enzyme trong phản ứng dịch chuyển điểm cắt hay kỹ thuật đánh dấu oligonucleotide và rẻ hơn các phương pháp khác. Tuy nhiên, lượng mẫu dò tạo ra lớn nhưng độ nhạy không cao.
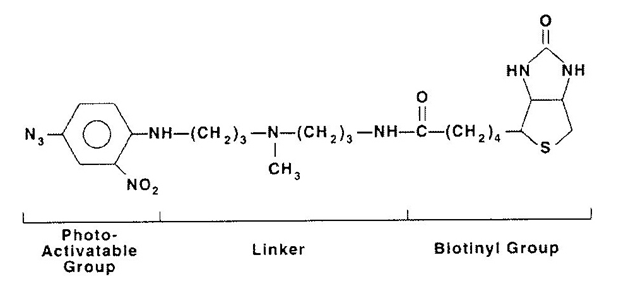
Photobiotin có công thức hóa học C23H35N9O45•C2H 4O2. Phân tử bao gồm một nhóm biotinyl, một nhóm nối (linker) cad một nhóm nitrophenyl azide.
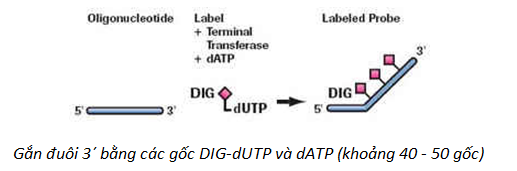
3.2.5. Đánh dấu đuôi (End Labeling)
Phương pháp này chủ yếu dùng cho đánh dấu mẫu dò oligonucleotide.
Ba phương pháp đánh dấu mẫu dò oligonucleotide với digoxigenin:


Bài viết khác
TƯ VẤN VÀ XÂY DỰNG PHÒNG THÍ NGHIỆM AN TOÀN